Кольори фізичних тіл, що нас оточують, визначаються поглинанням і відбиттям певних частин спектра атомами цих тіл. У попередньому параграфі йшлося про випромінювання та поглинання електромагнітного випромінювання атомами. Чи пов'язана ця нова інформація з кольором? І якщо так, то яким чином? Настав час розібратися. Наступні параграфи будуть присвячені з’ясуванню цих питань.
Що таке лінійчаті спектри випромінювання газів
Якщо кинути дрібочку кухонної солі в полум’я газового пальника, звичні блакитні язички одразу забарвляться в жовтий колір. Причина цього явища вам уже відома: до складу кухонної солі входить натрій, і саме цей метал має характерне жовте випромінювання. Розберемося в механізмі появи цього випромінювання. У полум’ї пальника натрій нагрівається, і електрони на верхніх оболонках атомів Натрію переходять у збуджений стан. Повертаючись на стаціонарну орбіту, електрони випромінюють електромагнітні хвилі, причому відповідно до постулатів Бора — чітко визначеної частоти.
Численні дослідження довели, що внаслідок нагрівання до високої температури пара будь-якої хімічної речовини випромінює світло, вузький пучок якого розкладається призмою на кілька пучків / ліній (рис. 51.1). Сукупність цих спостережуваних ліній називають лінійчатим спектром випускання. Зазначимо, що лінійчатий спектр випускання будь-якого конкретного хімічного елемента не збігається зі спектром випускання інших хімічних елементів і, відповідно, є «візитною карткою» елемента.
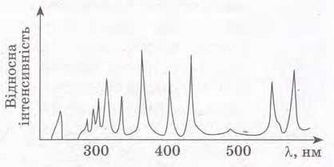
Рис. 51.1. Залежність відносної інтенсивності випромінювання від довжини хвилі. Схематичне зображення лінійчатого спектра елемента
Відбувається й зворотне явище: у випадку пропускання білого світла через пару речовини спостерігається виникнення темних ліній на тлі суцільного спектра. Темні лінії розташовані точно в тих місцях, де спостерігалися би світлі лінії спектра випускання цього хімічного елемента. Такий спектр називають лінійчатим спектром поглинання.
Чим відрізняються атомні та молекулярні спектри
Спектри молекулярних газів відрізняються від атомних спектрів і виглядають як система смуг із численних і дуже близьких одна до одної ліній. Така спектральна картина пояснюється двома причинами: коливаннями атомів усередині молекули та обертанням молекули.
Енергія коливального руху молекули теж підпорядковується законам квантової фізики й має дискретний ряд значень. Таким чином, один електронний енергетичний рівень розбивається на безліч коливальних підрівнів. Окрім коливань окремих частин молекули, може відбуватися обертання молекули як цілого.
У результаті електронні та коливальні рівні енергії молекули розбиваються на множину обертальних підрівнів. Кількість можливих переходів різко збільшується, що на практиці зумовлює виникнення величезної кількості ліній спектра, які зливаються в широкі смуги.:
Яким чином ініціюється рентгенівське випромінювання.
★ Роботи і. П. Пулюя^
У XXI ст. навряд чи знайдеться людина, яка хоча б раз у житті не робила рентгенівського знімка. Наприкінці ж XIX ст. зображення кисті людини з видимою структурою кісток (рис. 51.2.) обійшло шпальти газет усього світу й стало справжньою сенсацією для фізиків. Відкриття особливого проникного випромінювання німецький фізик Вільгельм Ксн рад Рентґен (1845-1923) здійснив 8 листопада 1895 р. Рентгенівське випромінювання виникає внаслідок взаємодії швидких електронів з атомами катода в рентгенівській трубці.
★ Розглянемо цей процес детальніше. Якщо енергія електронів достатньо значна, то може відбуватися вивільнення електронів із внутрішніх оболонок атомів із великим порядковим номером Z. «Повернення» електронів супроводжуватимуться випусканням дискретного спектра рентгенівського випромінювання, подібного до спектра у видимому діапазоні. Це випромінювання називають характеристичним рентгенівським випромінюванням. Крім того, у рентгенівській трубці відбувається гальмування швидких заряджених частинок під час їхньої взаємодії з електричними полями атомних ядер. Спектр такого випромінювання, яке дістало назву гальмівне рентгенівське випромінювання, є суцільним.

Значний внесок у дослідження рентгенівського випромінювання зробив видатний учений українського походження Іван Павлович Пу-люй (1845-1918). Фахівці, які займаються історією фіз'ики, досі сперечаються, хто насправді відкрив так звані «рентгенівські промені». Є достатньо свідчень, що саме Іван Пулюй уперше отримав докази практичного застосування цього випромінювання. Не втручаючись у цю дискусію на сторінках підручника, зазначимо, що беззаперечною є якість виконання досліджень українським ученим.
Як визначають хімічний склад речовини за результатами вимірювань атомних і рентгенівських спектрів
До цього ми розповідали про особливості атомних спектрів, було також приділено увагу фізичним теоріям, які пояснюють спостережувані факти. А чи замислювалися ви над тим, навіщо взагалі потрібні ці дослідження? Перша відповідь очевидна: для пізнання природи. А чи існує практичне застосування цих знань?
Уже зазначалося, що вимірювання спектрального випромінювання одноелсментних газів дозволяє ідентифікувати склад цих газів. Якщо порівняти інтенсивність цього виміру зі стандартом, то за відносним рівнем випромінювання можна визначити не тільки склад, але й концентрацію елемента. Прилади, що забезпечують такі вимірювання, називають спектрометрами (див. § 43 підручника).
На жаль, таким методом можна однозначно визначати лише одноелементні гази. Спектри ж молекулярних сполук складаються із широких смуг, із яких доволі важко виділити окремі лінії. Тому оптичні спектрометри можуть дати інформацію про структуру молекул лише за наявності добре розробленої методики інтерпретації результатів.
Однак у спеціальному випадку атомні спектри можуть допомогти в ідентифікації складних молекулярних сполук. При цьому реєструється характеристичне рентгенівське випромінювання, за яким можна не тільки виявити наявність елемента у молекулі, а й, порівнявши інтенсивність спектра з інтенсивністю стандартного зразка, визначити питомий уміст елемента в молекулі.
Підбиваємо підсумки
Атоми газоподібних речовин за підвищених температур випромінюють електромагнітні хвилі чітко визначених частот — у даному випадку йдеться про лінійчатий спектр випромінювання. Лінійчатий спектр кожного елемента характеризується індивідуальним для цього елемента набором частот.
Якщо газ опромінюють білим світлом, на спектрі спостерігаються чорні смуги безпосередньо на тих частотах, на яких відбувається випромінювання даного елемента,— у такому випадку йдеться про лінійчатий спектр поглинання.
Спектри випромінювання молекул відрізняються від аналогічних спектрів газів наявністю великої кількості близько розташованих ліній, які під час спостережень часто зливаються у смуги.
Під час взаємодії речовини з високоенергетичними електронами спостерігається рентгенівське випромінювання двох видів: характеристичне — індивідуальне для кожного елемента та гальмівне. Значний внесок у дослідження рентгенівського випромінювання зробив учений українського походження І. П. Пулюй.
Вимірювання атомних спектрів дозволяє одержати інформацію про елементний склад речовин.
Контрольні запитання
1. Що називають лінійчатим спектром випромінювання? лінійчатим спектром поглинання? 2. Назвіть характерні риси спектрального випромінювання молекул. ★ з. Назвіть різновиди рентгенівського випромінювання, що виникає внаслідок опромінення речовини високоенергетичними електронами. У чому відмінність цих різновидів? ★ 4. Який внесок зробив І. П. Пулюй у дослідження та використання рентгенівського випромінювання? ★ 5. Як за допомогою вимірювання атомних та рентгенівських спектрів можна одержати інформацію про елементний склад речовин?
Це матеріал з підручника Фізика 11 клас Бар'яхтар